 |
Es wird immer wichtiger, Zellen manipulieren zu können. Die Pharmakologie lebt vom Einbringen bestimmter Chemikalien in die Reaktionskreisläufe der Zelle. Medikamente müssen über die Zellmembran transportiert werden. Genetik heißt Veränderung des Zellgenoms. Dazu wird Erbmaterial in die Zelle eingeschleust. Man verwendet u.a. elektrische Methoden für den Stofftransport über Zellmembranen. Elektroporation ermöglicht das Permeabilisieren von Zellen. Stoffe können in das Zellinnere diffundieren. Elektrofusion initiiert die Vereinigung mehrerer Zellen. Deren Inhalte können dann frei miteinander wechselwirken.
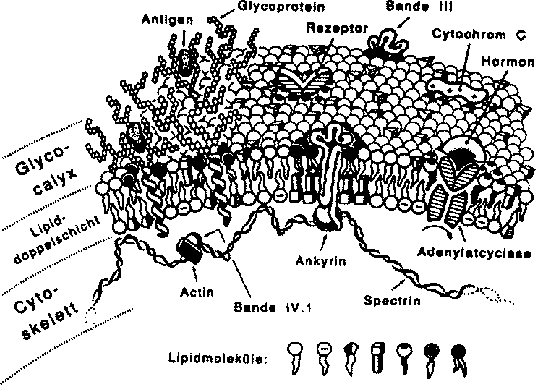
Zellmembranen (Abbildung 1) bestehen aus einer Vielzahl von Komponenten. Diese lassen sich in drei Klassen einteilen: Proteine, Lipide, Stützstrukturen.
Lipide bilden die Grundlage der Membran. Sie sind für die chemische und elektrische Isolation der Zelle gegen die Umgebung zuständig. Zusammensetzung und Struktur der Lipidschicht sind wesentlich für die physikalischen Eigenschaften der Zellmembran. Viele Proteine sind in der bimolekularen Lipidschicht gelöst. Sie stellen die Verbindung zu den Stützstrukturen wie Glycocalix und Actin-, Spektrin-, Fibringerüst dar. Funktion und Effektivität von Rezeptorproteinen, Transmembranporen, und anderen Proteinen werden wesentlich von den umgebenden Lipiden beeinflußt (Singer-Nicolson Modell [28]).Biologische Membranen sind in ihrer komplexen Zusammensetzung schwer zu untersuchen. Es gibt zwei Wege, zu einfacheren Modellsystemen zu kommen: Von der biologischen Seite her versucht man Zellen zu denaturieren. Wichtiges Beispiel ist die Arbeit mit Ghostzellen, z.B. in [6]. Der Zellinhalt, also Plasma, Kern und andere Organellen, wird gegen Pufferlösung ausgetauscht. Verwendet man einfach aufgebaute Zellen wie Erythrozyten, erhält man Vesikel mit biologischer, aber unzureichend bekannter Membranzusammensetzung und intaktem Stützgerüst. Von der anderen Seite her kann man mit Liposomen eines möglichst reinen Lipids beginnen. Die Lipidzusammensetzung kann biologischen Vorgaben angepaßt werden [24]. Genau bekannte Membranproteine und die Anbindung von Stützstrukturen rekonstituieren die Eigenschaften biologischer Membranen.
An diesen Modellsystemen kann man physikalische Eigenschaften biologischer Systeme studieren [13,43]. Mit Elektronenmikroskop oder AFM untersucht man die Anlagerung von Makromolekülen an die Membran. Man erhält Informationen über strukturelle Änderungen der Grenzfläche. Patch-Clamp-Versuche messen die Funktion einzelner Membrankanäle. Über das Einfügen von Fluorezensmarkern in die Membran sind Größen wie Beweglichkeit der Lipide oder Proteine, und Membranpotentiale zugänglich [7]. In Mikropipetten festgehaltene Vesikel ermöglichen das Messen von Membranviskosität und Oberflächenspannung [14,15,33,34].
In dieser Arbeit beschäftige ich mich mit planaren Lipiddoppelschichten. Wegen ihrer einfachen Geometrie sind sie elektrischen Meßmethoden leicht zugänglich. Spannungsverläufe über einer Lipidmembran lassen sich mit hoher zeitlicher Auflösung bei relativ geringem apparativen Aufwand messen.
Die Fläche des planaren Bilayers von ca. 1mm![]() macht ihn nicht
nur für die biophysikalische Grundlagenforschung interessant. Bei einer Dicke
von 4 bis 10nm hat man ein quasi zweidimensionales System zur
Verfügung. Beide Seiten der Membran sind frei zugänglich. Damit kann die
Zusammensetzung der wässrigen Phase asymmetrisch gewählt und verändert
werden. Bei Translokation oder asymmetrischer Anlagerung von Molekülen lassen
sich die Vorgänge auf den beiden Seiten der Membran gleichzeitig
untersuchen. Planare Lipidmembranen sind damit ideale Modellsysteme u.a. in
Pharmastudien oder Proteinfunktionsanalysen.
macht ihn nicht
nur für die biophysikalische Grundlagenforschung interessant. Bei einer Dicke
von 4 bis 10nm hat man ein quasi zweidimensionales System zur
Verfügung. Beide Seiten der Membran sind frei zugänglich. Damit kann die
Zusammensetzung der wässrigen Phase asymmetrisch gewählt und verändert
werden. Bei Translokation oder asymmetrischer Anlagerung von Molekülen lassen
sich die Vorgänge auf den beiden Seiten der Membran gleichzeitig
untersuchen. Planare Lipidmembranen sind damit ideale Modellsysteme u.a. in
Pharmastudien oder Proteinfunktionsanalysen.
Rißbildung in Oberflächen und Verhalten von Grenzflächen sind wichtige Forschungsgebiete in Physik und Chemie. Abgesehen vom grundlegenden Interesse an den physikalischen Eigenschaften von Zellmembran gibt es anwendungsbezogene Fragestellungen. Für das Verstehen und Weiterentwickeln von Techniken zur Elektroporation und Elektrofusion ist es notwendig, die Wirkung elektrischer Felder auf Membranen kennenzulernen. Jüngstes Beispiel ist die Diskussion um das Klonen erwachsener Tiere. Dort lag die Erfolgsrate bei der Übertragung der Zellkerne mittels Elektrofusion in vorbereitete Eizellen bei unter einem Promille [37]. Das dosierte Öffnen, längstmögliche Offenhalten und das sichere Ausheilen von Defekten kann an Modellsystemen studiert werden.
Es gibt keine experimentellen Daten zur Frühphase der Defektentstehung. Modelle werden nur mit Hilfe von Computersimulationen überprüft. Es fehlen Daten zum Einfluß des Stützgerüstes der Zellmembran auf ihre Stabilität gegenüber elektrischen Feldgradienten. Untersuchungen an reinen Lipiddoppelschichten müssen auf rekonstituierte Systeme ausgeweitet werden.
In dieser Arbeit wird die Kinetik des Aufweitens von Defekten in Lipidmembranen untersucht. Interessant ist das Entstehen von Defekten und der Mechanismus ihrer Ausdehnung. Welchen Einfluß hat die Randenergie auf Defektbildung und -ausweitung? Reine Lipidbilayer können mit einem artifiziellen Stützgerüst aus an die Membran polymerisiertem Actin zu Modellen für biologische Membranen rekonstituiert werden. Die dabei auftretenden Unterschiede im physikalischen Verhalten der Membran sind herauszufinden und zu erklären.